1. 裂解生物结构释放核酸的方法 :
核酸存在于生物结构内部,首先需要进行生物结构破解,进行核酸的释放。主要方法如下:
| 方法 | 机械裂解 | 酶裂解 | 化学裂解 |
| 原理 | 外力破坏结构 | 消化蛋白质或细胞、细菌、病毒结构 | 裂解液中的洗涤剂分解脂膜,释放结构内部成分。化学裂解缓冲液通常含有离液盐,如盐酸胍或尿素,这有助于破坏降解新暴露核酸蛋白质(如核酸酶)的稳定性,并使核酸与二氧化硅基质结合。化学裂解缓冲液的确切组成取决于应用方向和样品类型。 |
| 优势 | 效率高,速度快; 快速裂解缩短了从采集样本到分离核酸的时间; 适合于难以溶解的样品(例如植物材料、丝状真菌和酵母); | 无需机械裂解设备; 选择性的去除细胞壁,留下细胞部分采用另一种裂解方式(通常是化学裂解),方法灵活,避免了一些由机械裂解产生的破坏 | 价格便宜,操作简单,速度快;无需专用设备。 |
| 劣势 | 根据使用的方法,多样本处理时比较耗时(例如人工手动研磨处理); 大量样品处理耗时,可能会增加样品降解的风险; 机械处理会在样本中产生热量,导致蛋白质聚集和核酸降解; 需要一些特殊工具或仪器; | 耗时(酶消化可能需要1小时)而且价格昂贵; 由于酶诱导的细胞变化可能影响基因表达,因此不适合进行基因表达分析。 | 破坏细胞膜的洗涤剂通常也会溶解其他细胞膜,从而释放其成分。这种方法不适于细胞器特异性核酸的提取; 虽然这项技术对大肠杆菌有效,但对革兰氏阳性细菌、植物细胞或真菌细胞无效,因为存在阻止洗涤剂进入细胞膜的硬细胞壁; 在大肠杆菌样品中同时加入洗涤剂和离液盐可能会影响质粒DNA和基因组DNA的区别能力。 化学物质会给研究人员带来危险。 |
2. 核酸提取纯化 :
从生物结构中释放出来的核酸,与其他生物结构的碎片混合在一起,需要进行纯化,几种常见方法如下:
| 方法 | 有机提取 | 离心柱 | 磁珠 |
| 化学技术 | 通过酚类化合物分离 | 通过滤膜或位于离心柱试管底部的树脂进行分离 | 通过充当带电表面以吸引DNA的磁珠以及专为DNA分离而优化的试剂进行分离 |
| 样品类型 | • 细胞 • 组织 • 血液 • 植物样品 | • 所有样品类型 | • 所有样品类型 |
| 技术 | 化学试剂法 | 离心和真空辅助 | 无需液体转移的磁性分离 |
| 纯度 | 中 | 高 | 最高 |
| 通量 | 低通量 | 中高通量 | 高通量 |
| 优势 | • 高效裂解和分离 • 可扩展形式 • 非常适用于难处理样品 • 程序时间约30-60min | • 易于使用 • 可处理多种类型和体积的样品 • 产量和纯度高 | • 无堵塞风险 • 产量和效率高 • 重复性 • 收集快速 • 通过磁珠纯化仪自动处理 |
| 难点 | • 危险—需使用化学品通风橱 • 使用含氯有机试剂 • 费力 | • 容易堵塞 • 固定结合能力 | • 无堵塞风险 • 产量和效率高 • 重复性 • 收集快速 • 通过磁珠纯化仪自动处理 |
| 推荐使用 | • 大多数样品类型,但最适用于高脂肪含量组织(如脑组织和乳腺组织)或传染性样品的DNA提取 | • 离心柱——非常适用于中低通量处理(12-24个样品) • 96孔过滤板——非常适用于高通量处理 | • 高通量样品处理和自动化(>24个样品) |
<1>有机提取:
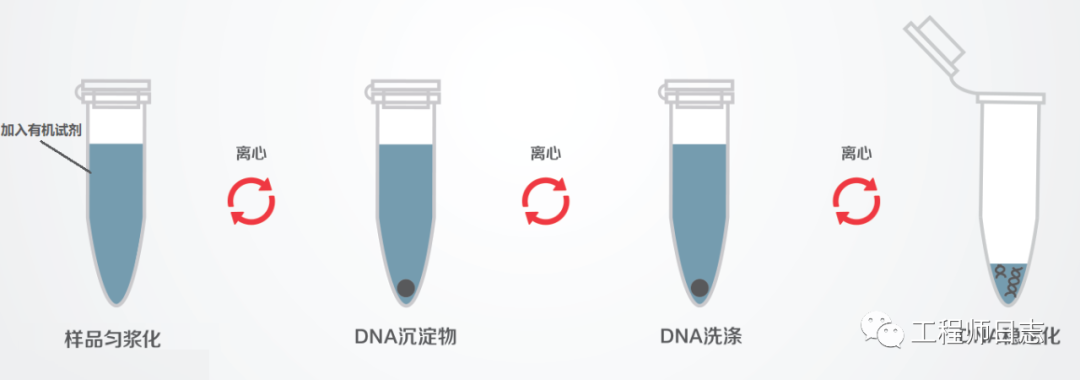
常见的有机提取如 苯酚-氯仿萃取
苯酚和氯仿均为有机溶剂,其萃取核酸原理是苯酚与氯仿对于与核酸结合的蛋白质有极强的变性作用,但对核酸本身没有影响。
经离心后,形成 上层水相 下层酚/氯仿相,变性后的蛋白质溶于酚/氯仿相或者在两相交界处形成凝胶层,而 核酸易溶于水 而 不溶于有机溶剂从而留在水相;同时,氯仿可以有助于有机相与水相的分离和去除溶于水的部分酚。最后,再将核酸通过乙醇沉淀即可达到提取的目的。
缺点是:
(1) 蛋白质难以彻底去除;
(2) 操作难度大且费时;
(3) 使用危险化学品
<2>离心柱法:
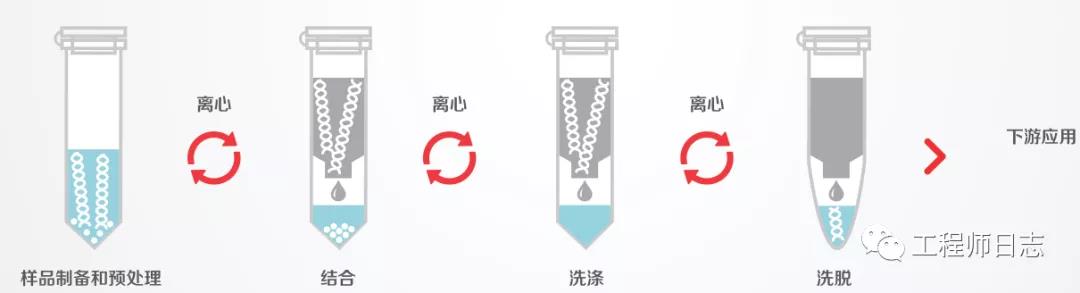
注:DNA 样本与离心柱发生吸附结合,样本的其他部分不会结合,被洗掉。洗涤结束后,用特定试剂,可将离心柱上的 DNA 洗脱,进行收集。
离心柱吸附 DNA 原理:
离心柱含有硅胶或专有树脂的固体基质,有官能基团固定在基质上,用于选择性结合核酸。
<3>磁珠吸附法:
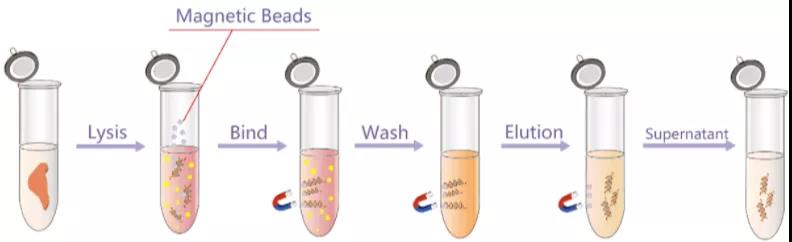
注:DNA 与磁珠结合在一起,磁铁将磁珠和 DNA 结合体吸住保留下来,上清液被吸走其他碎片。特定洗液,可将磁珠从 DNA 和磁珠的结合体上洗脱。最后仅剩下纯化后的 DNA。
磁珠吸附结合 DNA 原理:
磁珠基础结构分为三层,最内层的是聚苯乙烯,第二层包裹磁性物质(通常是Fe3O4),最外层是修饰的官能团(如羧基)。
其中官能团能与核酸结合,表面基团不同,下游的应用也不尽相同,如核酸提取,纯化,生物素捕获等。
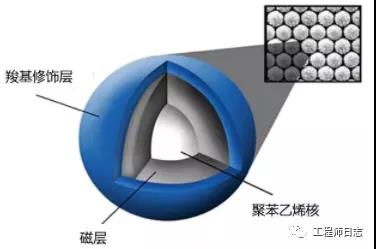
磁珠结构示意图
商业化磁珠产品体系一般包含:磁珠、聚乙二醇(PEG)、盐离子等。
基于SPRI(Solid Phase Reversible Immobilization )技术, DNA在一定浓度的PEG存在条件下,NaCl或MgCl2促进条件下,DNA分子构象会发生急剧变化,会暴露出磷酸骨架上大量的带负电荷的磷酸基团,与表面带负电荷的羧基磁珠结合。
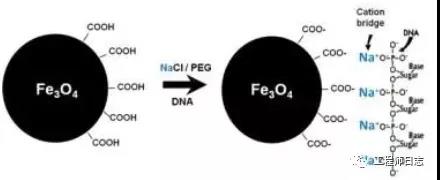
磁珠吸附结合 DNA
目前认为这种负负电荷间的作用是由于带正电荷的盐离子的作用(如Na+)。带负电磷酸基团借由解离的盐离子(如Na+)与羧基形成离子桥,使DNA被特异性吸附到羧基磁珠表面。利用磁珠的磁性,可通过外加磁场进行收集洗脱。
来源:工程师日志 ,作者pengfei zheng
声明:本平台注明来源的稿件均为转载,仅用于分享,不代表平台立场,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!






